
DESALEX
DESLORATADINA
Tabletas
, Caja,10-30 Tabletas,
Para visualizar el contenido completo de la IPPA (información para prescribir amplia), deberá iniciar sesión.
PRINCIPIO ACTIVO: Desloratadina es un polvo blanco a blancuzco ligeramente soluble en agua pero muy soluble en etanol, propilenglicol, cloruro de metileno, metanol y octanol. Tiene como fórmula empírica: C19H19CIN2 y Peso Molecular de 310.8. El nombre químico es 8-cloro-6,11-dihidro-11-(4-piperidinilideno)-5H-benzo-[5,6] ciclohepta [1,2-b]piridina y tiene la siguiente fórmula estructural:
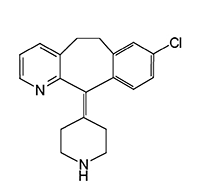
Desloratadina (SCH 34117)
DESALEX® TABLETAS
DESALEX® Tabletas contiene 5 mg de desloratadina micronizada.
DESALEX® JARABE
Cada ml de DESALEX® jarabe contiene 0.5 mg de desloratadina.
INDICACIONES Y USO: DESALEX® está indicado en el control rápido y efectivo de los síntomas asociados con rinitis alérgica, tales como: estornudos, rinorrea, congestión y prurito nasal; como también, prurito, lagrimeo, ardor y enrojecimiento ocular y en el prurito del paladar. Adicionalmente, como terapia en rinitis alérgica asociada con asma.
DESALEX® también está indicado en el control de los síntomas y signos de urticaria como son el prurito, el tamaño y número de las ronchas o habones.
PROPIEDADES FARMACODINÁMICAS: En un programa clínico, la desloratadina demostró ser segura y eficaz en el tratamiento de los síntomas asociados con rinitis alérgica. Adicionalmente, se demostró la seguridad y eficacia de desloratadina en el tratamiento de los síntomas de urticaria crónica idiopática y otros trastornos dermatológicos.
En un estudio en el cual fue administrada desloratadina a dosis de 45 mg al día (nueve veces la dosis clínica) por diez días, no se observó prolongación del intervalo QTc.
Desloratadina no penetra fácilmente el sistema nervioso central. A la dosis recomendada de 5mg al día para adultos y adolescentes, no hubo exceso de incidencia de somnolencia en comparación con el placebo. Desloratadina administrada como una dosis única al día de 7.5 mg en adultos y adolescentes no afectó el desempeño psicomotor en estudios clínicos, ni una sola dosis diaria de
5 mg en adultos afecta a las medidas estándar de desempeño de pilotaje en condiciones de simulación de vuelo. La influencia de desloratadina es nula o insignificante sobre la habilidad para conducir y usar máquinas.
No se observaron cambios clínicos relevantes en las concentraciones plasmáticas de desloratadina en estudios de interacción con dosis múltiples de azitromicina, ketoconazol, eritromicina, fluoxetina o cimetidina.
CONTRAINDICACIONES: Hipersensibilidad a la sustancia activa o a cualquiera de sus componentes. Embarazo y lactancia.
USO DURANTE EL EMBARAZO Y EL PERIODO DE LACTANCIA: No se observaron efectos de la Desloratadina sobre la fertilidad en ratas, incluso a una exposición hasta 34 veces mayor que en el humano, a la dosis clínica recomendada.
No se observaron efectos teratógenos ni mutagénicos en estudios en animales realizados con desloratadina (ver Toxicología Preclínica). Dado que no se cuenta con información clínica sobre la seguridad de la desloratadina durante el embarazo, DESALEX® no debe usarse durante el embarazo a menos que los beneficios potenciales superen ampliamente los riesgos.
La desloratadina se excreta por la leche materna; por consiguiente, no se recomienda DESALEX® en mujeres en periodo de lactancia.
EVENTOS ADVERSOS: A la dosis recomendada de 5 mg, los eventos adversos reportados con mayor incidencia que el placebo incluyeron boca seca, fatiga y dolor de cabeza.
Casos muy raros de reacciones de hipersensibilidad, incluyendo anafilaxis y erupción cutánea, han sido reportados durante la comercialización de desloratadina. Adicionalmente, casos de taquicardia, palpitaciones, convulsiones, hiperactividad psicomotora, somnolencia, elevación de las enzimas hepáticas y bilirrubina, y hepatitis han sido reportados muy raramente.
EFECTOS SOBRE LA CAPACIDAD DE CONDUCIR VEHÍCULOS Y USAR MAQUINARIA: No se han observado efectos sobre la capacidad para conducir vehículos y usar maquinaria (ver Propiedades farmacodinámicas), sin embargo se recomienda hacer un llamado al cuidado en los pacientes que requieran ánimo vigilante.
INTERACCIONES FARMACOLÓGICAS: No se han observado interacciones farmacológicas clínicamente significativas en los estudios clínicos con la administración concomitante de azitromicina, eritromicina, ketoconazol, fluoxetina o cimetidina. No hubo efecto de la comida o del jugo de toronja en la absorción de la desloratadina.
Cuando se administra concomitantemente con alcohol, DESALEX® no potencializa los efectos de deterioro del desempeño psicomotor debidos al alcohol (ver Propiedades farmacodinámicas).
FARMACOLOGÍA CLÍNICA:
Propiedades farmacocinéticas: Desloratadina se absorbe bien, alcanzando la concentración plasmática máxima aproximadamente a las 3 horas; la fase terminal de la vida media de eliminación es de aproximadamente 27 horas. El grado de acumulación de desloratadina es consistente con su vida media y con una frecuencia de administración de una vez al día. La biodisponibilidad de desloratadina es proporcional a la dosis entre el rango de 5 mg a 20 mg.
Desloratadina se une moderadamente a las proteínas plasmáticas (82 a 88%).
Desloratadina es metabolizada extensamente a 3-hidroxi desloratadina, un metabolito activo, el cual más tarde es glucuronizado. Un estudio en seres humanos de balance de masas documentó una recuperación de aproximadamente el 87% de la dosis de 14C-desloratadina, la cual fue distribuida de forma equitativa en orina y heces como productos metabólicos.
El perfil farmacocinético de desloratadina es comparable en adultos voluntarios sanos y voluntarios sanos geriátricos y no se requiere ajuste de dosis.
En estudios de dosis única de desloratadina tabletas (7.5 mg) y jarabe (5 mg), no hubo efecto de los alimentos en la disposición de desloratadina. En otro estudio, el jugo de toronja no tuvo efecto en la disposición de desloratadina.
En estudios cruzados de desloratadina, en dosis única, las formulaciones de tabletas y jarabe fueron bioequivalentes.
ADVERTENCIAS Y PRECAUCIONES: No se ha establecido la eficacia ni la seguridad de DESALEX® Tabletas en niños menores de 12 años de edad y de DESALEX® Jarabe en niños menores de 6 meses de edad.
DOSIS Y ADMINISTRACIÓN:
Adultos y niños mayores de 12 años: 1 tableta (5 mg) de DESALEX® o 2 cucharaditas (10 ml) de DESALEX® Jarabe, una vez al día, independientemente de las comidas para el alivio de los síntomas asociados con la rinitis alérgica (incluyendo rinitis alérgica intermitente y persistente) y con la urticaria. Para uso oral.
Niños de 6 a 11 años de edad: 5 ml (2,5 mg) de DESALEX® Jarabe, una vez al día, independientemente de las comidas para el alivio de los síntomas asociados con la rinitis alérgica (incluyendo rinitis alérgica intermitente y persistente) y con la urticaria. Para uso oral.
Niños de 1 a 5 años de edad: 2,5 ml (1,25 mg) de DESALEX® Jarabe, una vez al día, independientemente de las comidas para el alivio de los síntomas asociados con la rinitis alérgica (incluyendo rinitis alérgica intermitente y persistente) y con la urticaria. Para uso oral.
Niños de 6 a 11 meses de edad: 2 ml (1 mg) de DESALEX® Jarabe, una vez al día, independiente de las comidas para el alivio de los síntomas asociados con la rinitis alérgica (incluyendo rinitis alérgica intermitente y persistente) y con la urticaria. Para uso oral.
La rinitis alérgica intermitente (presencia de síntomas por menos de 4 días a la semana o por menos de 4 semanas) debe ser manejada de acuerdo con la evaluación de la historia de la enfermedad del paciente y el tratamiento podría ser descontinuado después de la resolución de los síntomas y reiniciado cuando reaparezcan. En la rinitis alérgica persistente (presencia de síntomas por 4 días o más a la semana y por más de 4 semanas), el tratamiento continuo puede proponerse a los pacientes durante periodos prolongados de exposición a alérgenos.
SOBREDOSIS: En caso de una sobredosis, se debe instaurar tratamiento general para remover la sustancia activa no absorbida. Se recomienda tratamiento sintomático y de apoyo. Desloratadina no se elimina por hemodiálisis.
ABUSO DE SUSTANCIAS Y DEPENDENCIA: No existe información que indique que ocurre abuso o dependencia con desloratadina tabletas.
INFORMACIÓN PRECLÍNICA:
Propiedades farmacodinámicas: Desloratadina, el principio activo en DESALEX® tabletas y Jarabe, es un antihistamínico con actividad antagonista selectiva sobre el receptor periférico H1.
Adicionalmente a la actividad antihistamínica, desloratadina ha demostrado actividad antialérgica en estudios in vitro (conducidos en células humanas) e in vivo. Estos estudios han mostrado que desloratadina puede inhibir eventos en cascada de inflamación alérgica, incluyendo:
• Liberación de citoquinas proinflamatorias: IL-4, IL-6, IL-8 e IL-13 de las células humanas mastocitos/basófilos.
• Expresión de moléculas de adhesión, como la selectina P.
• Inhibición de tos alérgica en modelos animales.
ESTUDIOS PRECLÍNICOS: Desloratadina es el principal metabolito activo de la loratadina. Los estudios preclínicos conducidos con desloratadina no revelan un riesgo especial para los seres humanos según estudios de genotoxicidad, potencial carcinogénico, y toxicidad sobre la reproducción.
DESCRIPCIÓN DEL PRODUCTO: Cada TABLETA de DESALEX®, contiene 5,0 mg de desloratadina. Cada 1 ml de DESALEX® JARABE contiene 0,5 mg de desloratadina.
Desloratadina es un antihistamínico no sedante con actividad antagonista selectiva sobre los receptores periféricos H1. DESALEX® Jarabe no contiene azúcar, colorantes ni alcohol.
PRESENTACIÓN: DESALEX® Tabletas, caja por 10 y 30 tabletas (Reg. San. INVIMA 2012M-0000720-R1). DESALEX® Jarabe, frasco por 15 ml, 60 ml y 120 ml. (Reg. San. INVIMA 2013M-0001703-R1).
Este documento fue revisado por última vez en Noviembre de 2014.
S-CCDS-MK4117-MTL-112014
MERCK SHARP & DOHME
Bogotá, D.C. - Colombia
CONDICIONES DE ALMACENAMIENTO: Almacenar a temperatura inferior a 30°C.